Proč klasické léky selhávají
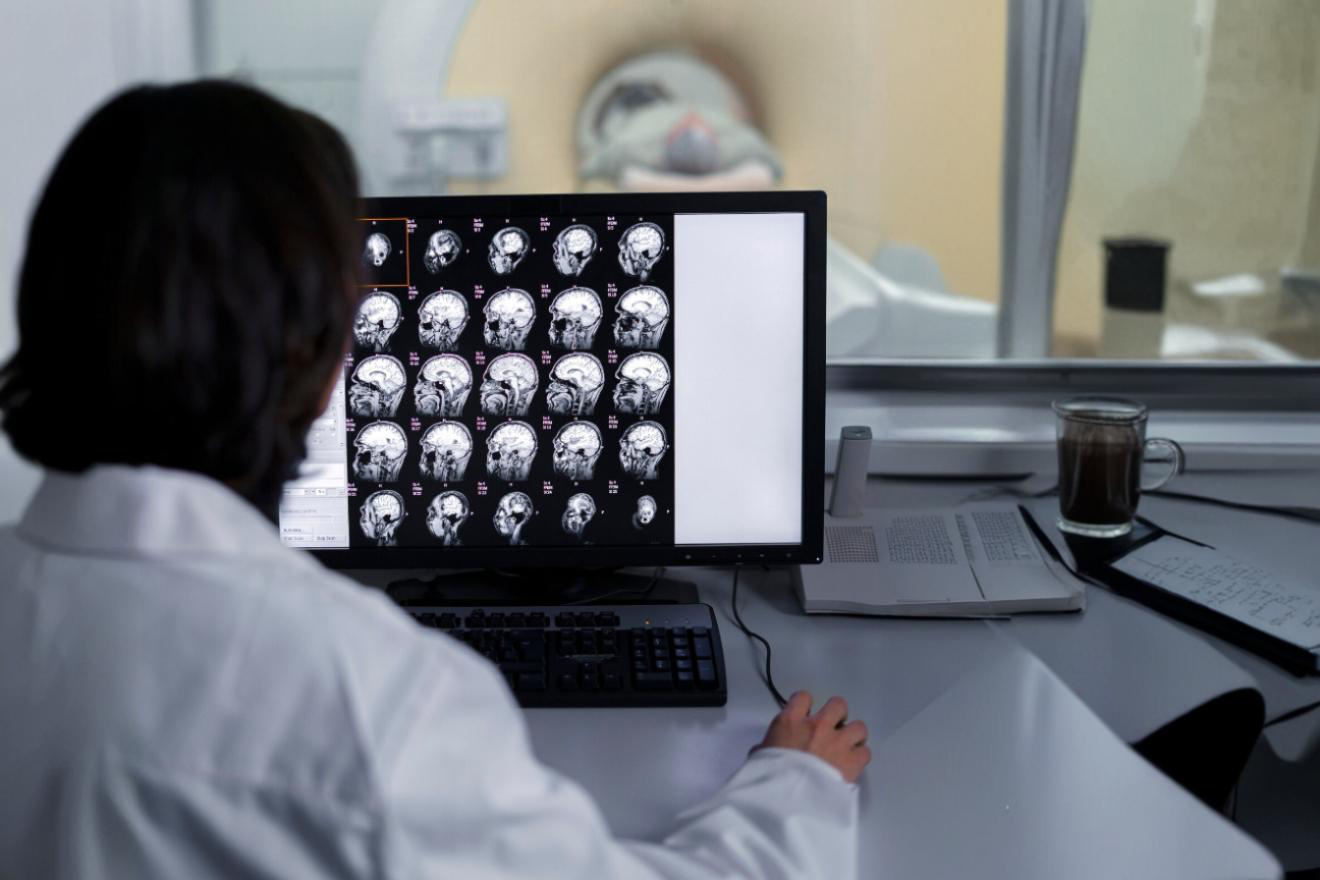
Mozek je mimořádně chráněný orgán a tato ochrana mu v případě léčby komplikuje život. Hematoencefalická bariéra funguje jako přísný vrátný, který do mozku nepustí většinu léčivých látek. Ty malé molekuly, které projdou, se navíc rychle vyplaví z organismu, než stihnou zabrat.
Přidejte k tomu riziko nežádoucích účinků v jiných tkáních a máte jasno, proč tradiční léčba neurodegenerativních chorob naráží na limity. Farmaceutické firmy vyvíjejí stovky přípravků, ale jen zlomek z nich dokáže efektivně překonat bariéru a dosáhnout postižených neuronů.
Co přinášejí nanočástice
Nanomedikamenty jsou inženýrsky navržené částice v nanometrovém měřítku, které dokážou léčivo ochránit a dopravit přesně na cílové místo. Představte si je jako miniaturní kontejnery, které mají na povrchu speciální značky umožňující průchod hematoencefalickou bariérou.
Tyto nanočástice navíc dokážou kontrolovaně uvolňovat léčivo v čase, což zajišťuje optimální koncentraci v mozku bez zbytečného zatížení organismu. Samotná konstrukce částic je však jen polovina úspěchu. Bez možnosti sledovat, kam se nanomedikamenty dostávají a jak fungují, by lékaři postupovali naslepo.
Role zobrazovacích metod a strojového učení
Tady vstupuje do hry kombinace molekulárního zobrazování, jako je MRI nebo PET, se strojovým učením. Tyto technologie umožňují sledovat v reálném čase, kam přesně se nanočástice dostávají, kolik jich dorazí do cílové tkáně a jaký mají biologický účinek.
Algoritmy umělé inteligence pak analyzují data ze zobrazování a pomáhají optimalizovat parametry nanomedikamentů. Výzkumníci tak mohou přizpůsobit velikost částic, typ povrchového povlaku, způsob cílení nebo kinetiku uvolňování léčiva. Jde o iterativní proces: návrh, zobrazení, analýza AI, úprava návrhu.
Personalizace podle jednotlivých pacientů
Každý pacient s Alzheimerovou nebo Parkinsonovou chorobou má trochu odlišný průběh nemoci. AI modely trénované na zobrazovacích datech od konkrétních pacientů nebo ze zvířecích studií dokážou předpovědět, která formulace nanomedikamentu bude fungovat nejlépe v daném biologickém kontextu.
Výzkumný tým z Národního institutu duševního zdraví v Česku například zjistil, že nanočástice vypadající slibně v laboratorních podmínkách měly ve skutečnosti mnohem horší distribuci v živé tkáni. Teprve zobrazovací metody tento problém odhalily. Následná analýza pomocí AI ukázala vzorce v distribuci nanočástic napříč různými oblastmi mozku a výzkumníci mohli upravit architekturu částic.
Praktické aplikace a budoucnost
Tým vědců aktuálně pracuje na nanoformulaci nazývané molekulární nanoroboti, kterou lze aplikovat formou nosního spreje. Paralelně vyvíjejí algoritmy strojového učení pro predikci optimálního dávkování léčiva.
Další projekt zahrnuje AI model využívající obrazové vzorce z kohort pacientů s Alzheimerovou a Parkinsonovou chorobou k vyladění parametrů doručování léčiva. Výzkumníci spolupracují s klinickými lékaři na definování zobrazovacích ukazatelů, které budou relevantní pro regulatorní schválení. Cílem je posunout léčbu od pouhého zvládání příznaků k faktické modifikaci průběhu nemoci.
Co brání širšímu nasazení
Technologie má velký potenciál, ale před masovým využitím stojí řada překážek. Mezi hlavní patří bezpečnost částic, jejich dlouhodobá akumulace v organismu a možné imunitní reakce.
Výrobní proces musí být škálovatelný a splňovat regulatorní požadavky. Chybí také sdílené databáze zobrazovacích dat pro trénink AI modelů a jednotné standardy. Výzkumníci otevřeně přiznávají, že heterogenita pacientů představuje výzvu pro robustní algoritmy strojového učení.
Proč je interdisciplinární spolupráce klíčová
Úspěch celého přístupu závisí na propojení více oborů. Materiáloví vědci navrhují nanočástice, specialisté na zobrazování dodávají data, experti na AI vytváří prediktivní modely a kliničtí lékaři definují, co skutečně pomůže pacientům.
Představte si budoucnost, kdy pacient s ranou diagnózou neurodegenerativního onemocnění dostane infuzi nanomedikamentu. Lékař následně pořídí MRI snímek, vloží ho do AI modelu, který navrhne úpravu další dávky, a terapii tak průběžně vylaďuje podobně jako ladění hudebního nástroje. Stavební bloky pro tento scénář už existují, zbývá je propojit do funkčního celku.
Zdroj: Phys.org